Maailm, milles me elame, on kujuteldamatult ilus ja täis palju erinevaid protsesse, mis määravad elu kulgu. Kõiki neid protsesse uurib tuttav teadus - füüsika. See annab võimaluse saada vähem alt aimu universumi päritolust. Selles artiklis käsitleme sellist mõistet nagu molekulaarkineetiline teooria, selle võrrandid, tüübid ja valemid. Enne nende küsimuste põhjalikuma uurimise juurde asumist peate siiski enda jaoks selgeks tegema füüsika ja selle uuritavate valdkondade tähenduse.
Mis on füüsika?

Tegelikult on see väga ulatuslik teadus ja võib-olla üks kõige põhjapanevamaid inimkonna ajaloos. Näiteks kui sama arvutiteadus on seotud peaaegu kõigi inimtegevuse valdkondadega, olgu selleks siis arvutuslik disain või koomiksite loomine, siis füüsika on elu ise, selle keeruliste protsesside ja voogude kirjeldus. Proovime välja mõelda selle tähenduse, lihtsustades mõistmist nii palju kui võimalik.
NiiSeega on füüsika teadus, mis tegeleb energia ja mateeria, nendevaheliste seoste uurimisega, paljude meie tohutus universumis toimuvate protsesside selgitamisega. Aine struktuuri molekulaarkineetiline teooria on vaid väike langus teooriate ja füüsikaharude meres.
Energiat, mida see teadus üksikasjalikult uurib, saab esitada mitmel erineval kujul. Näiteks valguse, liikumise, gravitatsiooni, kiirguse, elektri ja paljude muude vormide näol. Selles artiklis käsitleme nende vormide struktuuri molekulaarkineetilist teooriat.
Aine uurimine annab meile aimu aine aatomistruktuurist. Muide, see tuleneb molekulaarkineetilisest teooriast. Aine ehitusteadus võimaldab meil mõista ja leida oma olemasolu mõtet, elu tekkimise põhjuseid ja Universumit ennast. Proovime siiski uurida aine molekulaarkineetilist teooriat.
Esiteks, terminoloogia ja võimalike järelduste täielikuks mõistmiseks on vaja sissejuhatust.
Füüsika teemad
Vastates küsimusele, mis on molekulaarkineetiline teooria, ei saa jätta rääkimata füüsika osadest. Igaüks neist käsitleb inimelu konkreetse valdkonna üksikasjalikku uurimist ja selgitamist. Need on klassifitseeritud järgmiselt:
- Mehaanika, mis on jagatud veel kaheks osaks: kinemaatika ja dünaamika.
- Staatiline.
- Termodünaamika.
- Molekulaarne sektsioon.
- Elektrodünaamika.
- Optika.
- Kvantide ja aatomituuma füüsika.
Räägime konkreetselt molekulaarsestfüüsika, sest see põhineb molekulaarkineetilisel teoorial.
Mis on termodünaamika?
Üldiselt on molekulaarne osa ja termodünaamika omavahel tihed alt seotud füüsikaharud, mis uurivad eranditult füüsikaliste süsteemide koguarvu makroskoopilist komponenti. Tasub meeles pidada, et need teadused kirjeldavad täpselt kehade ja ainete sisemist seisundit. Näiteks nende olek kuumutamisel, kristalliseerumisel, aurustumisel ja kondenseerumisel aatomitasandil. Teisisõnu, molekulaarfüüsika on teadus süsteemidest, mis koosnevad tohutul hulgal osakestest: aatomitest ja molekulidest.
Need teadused uurisid molekulaarkineetilise teooria põhisätteid.
Juba seitsmenda klassi käigus tutvusime mõistetega mikro- ja makromaailm, süsteemid. Ei ole üleliigne neid termineid mälus värskendada.
Mikromaailm, nagu näeme juba selle nimest, koosneb elementaarosakestest. Teisisõnu, see on väikeste osakeste maailm. Nende suurusi mõõdetakse vahemikus 10-18 m kuni 10-4 m ja nende tegeliku oleku aeg võib ulatuda nii lõpmatuseni kui ka ebaproportsionaalselt väikesed intervallid, näiteks 10-20 s.
Makromaailm käsitleb stabiilsete vormidega kehasid ja süsteeme, mis koosnevad paljudest elementaarosakestest. Sellised süsteemid on vastavuses meie inimese suurusega.
Lisaks on olemas selline asi nagu megamaailm. See koosneb tohututest planeetidest, kosmilistest galaktikatest ja kompleksidest.
Põhitõedteooria
Nüüd, kui oleme veidi kokkuvõtet teinud ja füüsika põhimõisteid meelde jätnud, võime minna otse selle artikli peateema juurde.
Molekulaarkineetiline teooria ilmus ja sõnastati esimest korda 19. sajandil. Selle olemus seisneb selles, et see kirjeldab üksikasjalikult mis tahes aine struktuuri (sagedamini gaaside kui tahkete ja vedelate kehade struktuuri), mis põhineb kolmel põhisättel, mis koguti selliste silmapaistvate teadlaste eeldustest nagu Robert Hooke, Isaac. Newton, Daniel Bernoulli, Mihhail Lomonosov ja paljud teised.
Molekulaarkineetilise teooria peamised sätted kõlavad järgmiselt:
- Absoluutselt kõik ained (olenemata sellest, kas need on vedelad, tahked või gaasilised) on keeruka struktuuriga, mis koosnevad väiksematest osakestest: molekulidest ja aatomitest. Aatomeid nimetatakse mõnikord "elementaarmolekulideks".
- Kõik need elementaarosakesed on alati pidevas ja kaootilises liikumises. Igaüks meist on kohanud selle ettepaneku otsest tõestust, kuid tõenäoliselt ei omistanud ta sellele erilist tähtsust. Näiteks nägime kõik päikesekiirte taustal, et tolmuosakesed liiguvad pidev alt kaootilises suunas. See on tingitud asjaolust, et aatomid tekitavad üksteisega vastastikuseid tõuke, andes üksteisele pidev alt kineetilist energiat. Seda nähtust uuriti esmakordselt 1827. aastal ja see sai nime avastaja järgi - "Browni liikumine".
- Kõik elementaarosakesed on üksteisega pidevas interaktsioonisteatud jõud, millel on elektriline kivim.
Väärib märkimist, et teine näide, mis kirjeldab positsiooni number kaks, mis võib kehtida ka näiteks gaaside molekulaarkineetilise teooria kohta, on difusioon. Me puutume sellega kokku igapäevaelus ning paljudes katsetes ja kontrollides, seega on oluline omada sellest ettekujutust.
Esm alt kaaluge järgmisi näiteid:
Arst kallas kogemata laual olevast kolbast alkoholi. Või kukkusite parfüümipudeli maha ja see levis üle kogu põranda.
Miks nendel kahel juhul täidavad nii alkoholi- kui parfüümilõhn mõne aja pärast kogu ruumi, mitte ainult seda piirkonda, kuhu nende ainete sisu maha voolas?
Vastus on lihtne: difusioon.
Difusioon - mis see on? Kuidas see voolab?

See on protsess, mille käigus ühe konkreetse aine (tavaliselt gaasi) moodustavad osakesed tungivad teise aine molekulidevahelisse tühimikesse. Meie ül altoodud näidetes juhtus järgmine: termilise, st pideva ja dissotsieerunud liikumise tõttu langesid alkoholi ja/või parfüümi molekulid õhumolekulide vahedesse. Järk-järgult, aatomite ja õhumolekulidega kokkupõrke mõjul, levivad nad ruumis laiali. Muide, difusiooni intensiivsus, see tähendab selle voolu kiirus, sõltub difusioonis osalevate ainete tihedusest, samuti nende aatomite ja molekulide liikumisenergiast, mida nimetatakse kineetiliseks. Mida suurem on kineetiline energia, seda suurem on nende molekulide kiirus ja intensiivsus.
Kiireimat difusiooniprotsessi võib nimetada difusiooniks gaasides. Selle põhjuseks on asjaolu, et gaas ei ole oma koostiselt homogeenne, mis tähendab, et molekulidevahelised tühimikud gaasides hõivavad vastav alt märkimisväärsel hulgal ruumi ning võõrkeha aatomite ja molekulide neisse viimise protsess kulgeb lihtsam alt ja kiiremini..
Vedelike puhul on see protsess veidi aeglasem. Suhkrukuubikute lahustumine teekruusis on vaid näide tahke aine difusioonist vedelikus.
Kuid kõige pikem aeg on difusioon tahke kristalse struktuuriga kehades. See on täpselt nii, sest tahkete ainete struktuur on homogeenne ja tugeva kristallvõrega, mille rakkudes vibreerivad tahke aine aatomid. Näiteks kui kahe metallvarda pinnad puhastada hästi ja seejärel üksteisega kokku puutuda, siis suudame piisav alt pika aja pärast tuvastada ühe metalli tükke teises ja vastupidi.
Nagu iga teinegi põhiosa, on ka füüsika põhiteooria jagatud eraldi osadeks: klassifikatsioon, tüübid, valemid, võrrandid jne. Seega oleme õppinud molekulaarkineetilise teooria põhitõdesid. See tähendab, et võite julgelt jätkata üksikute teoreetiliste plokkide kaalumist.
Gaaside molekulaarkineetiline teooria
Gaasi teooria sätteid on vaja mõista. Nagu me varem ütlesime, käsitleme gaaside makroskoopilisi omadusi, nagu rõhk ja temperatuur. See onSeda on hiljem vaja gaaside molekulaarkineetilise teooria võrrandi tuletamiseks. Aga matemaatika - hiljem ja nüüd tegeleme teooria ja vastav alt ka füüsikaga.
Teadlased on sõnastanud viis gaaside molekulaarteooria sätet, mis aitavad mõista gaaside kineetilist mudelit. Need kõlavad järgmiselt:
- Kõik gaasid koosnevad elementaarosakestest, millel ei ole teatud suurust, kuid millel on kindel mass. Teisisõnu, nende osakeste maht on nendevahelise pikkusega võrreldes minimaalne.
- Gaasi aatomitel ja molekulidel praktiliselt puudub potentsiaalne energia, vastav alt seadusele on kogu energia võrdne kineetilisega.
- Selle seisukohaga tutvusime juba varem - Browni liikumine. See tähendab, et gaasiosakesed on alati pidevas ja kaootilises liikumises.
- Absoluutselt kõik gaasiosakeste vastastikused kokkupõrked, millega kaasneb kiiruse ja energia sõnum, on täiesti elastsed. See tähendab, et kokkupõrke ajal ei esine energiakadu ega järske hüppeid nende kineetilises energias.
- Norma altingimustes ja püsival temperatuuril on peaaegu kõigi gaaside osakeste liikumise keskmine energia sama.
Vienda positsiooni saame seda tüüpi gaaside molekulaarkineetilise teooria võrrandi abil ümber kirjutada:
E=1/2mv^2=3/2kT, kus k on Boltzmanni konstant; T - temperatuur kelvinites.
See võrrand võimaldab meil mõista seost gaasi elementaarosakeste kiiruse ja nende absoluutse temperatuuri vahel. Seega, mida kõrgem on nende absoluuttemperatuur, seda suurem on nende kiirus ja kineetiline energia.
Gaasirõhk
Selliseid karakteristiku makroskoopilisi komponente, nagu gaaside rõhk, saab selgitada ka kineetilise teooria abil. Selleks kujutame ette järgmist näidet.
Oletame, et mingi gaasi molekul on kastis, mille pikkus on L. Kasutame ülalkirjeldatud gaasiteooria sätteid ja arvestame sellega, et molekulaarsfäär liigub ainult piki x -telg. Nii saame jälgida elastse kokkupõrke protsessi ühe anuma (kasti) seinaga.
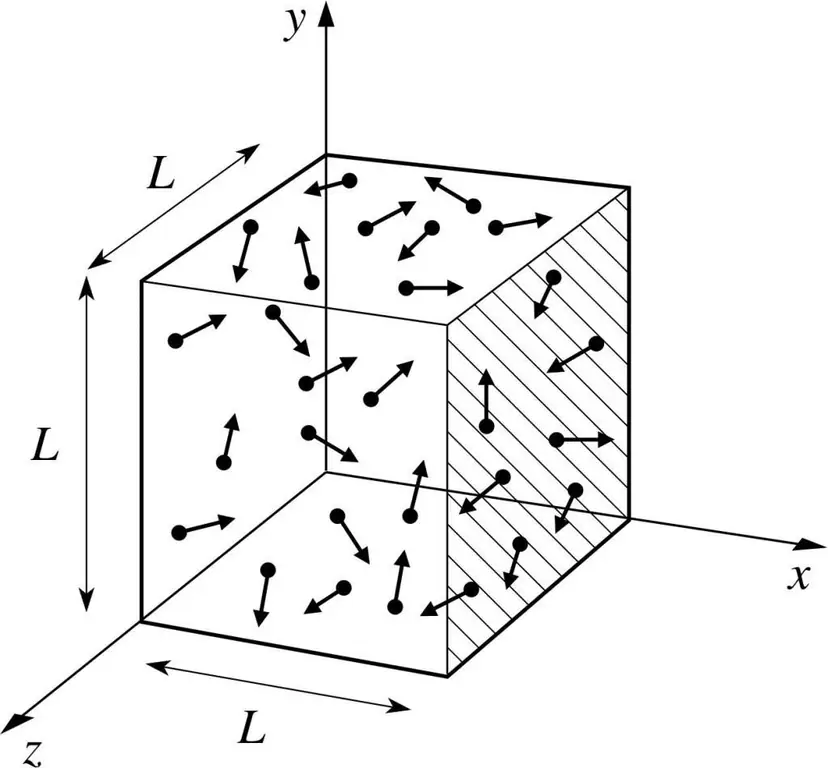
Käimasoleva kokkupõrke impulss, nagu me teame, määratakse valemiga: p=mv, kuid sel juhul võtab see valem projektsioonikuju: p=mv(x).
Kuna me arvestame ainult x-telje ehk x-telje dimensiooni, väljendatakse kogu impulsi muutust valemiga: mv(x) - m(-v(x))=2mv(x).
Järgmisena kaaluge meie objekti poolt avaldatavat jõudu, kasutades Newtoni teist seadust: F=ma=P/t.
Nendest valemitest väljendame gaasipoolse rõhu: P=F/a;
Nüüd asendame jõuavaldise saadud valemiga ja saame: P=mv(x)^2/L^3.
Pärast seda saab meie valmis rõhuvalemi kirjutada N-nda arvu gaasimolekulide jaoks. Teisisõnu näeb see välja selline:
P=Nmv(x)^2/V, kus v on kiirus ja V on helitugevus.
Nüüd proovime välja tuua mõned gaasirõhu põhisätted:
- See avaldub läbimolekulide kokkupõrked selle objekti seinte molekulidega, milles see asub.
- Rõhu suurus on otseselt võrdeline molekulide anuma seintele mõjuva jõu ja kiirusega.
Mõned lühikesed järeldused teooria kohta
Enne kui läheme kaugemale ja kaalume molekulaarkineetilise teooria põhivõrrandit, pakume teile mõned lühikesed järeldused ül altoodud punktidest ja teooriast:
- Selle aatomite ja molekulide keskmise liikumisenergia mõõt on absoluutne temperatuur.
- Kui kaks erinevat gaasi on samal temperatuuril, on nende molekulidel sama keskmine kineetiline energia.
- Gaasiosakeste energia on otseselt võrdeline keskmise ruutkiirusega: E=1/2mv^2.
- Kuigi gaasimolekulidel on vastav alt keskmine kineetiline energia ja keskmine kiirus, liiguvad üksikud osakesed erineva kiirusega: mõned kiiresti, mõned aeglaselt.
- Mida kõrgem on temperatuur, seda suurem on molekulide kiirus.
- Mitu korda tõstame gaasi temperatuuri (näiteks kahekordistame), sama palju suureneb selle osakeste liikumisenergia (vastav alt kahekordistub).
Põhivõrrand ja valemid

Molekulaarkineetilise teooria põhivõrrand võimaldab teil luua seose mikromaailma suuruste ja vastav alt makroskoopiliste ehk mõõdetud suuruste vahel.
Üks lihtsamaid mudeleid, mida molekulaarteooria võib kaaluda, on ideaalne gaasimudel.
Võib nii öeldasee on omamoodi kujuteldav mudel, mida uurib ideaalse gaasi molekulaarkineetiline teooria, milles:
- lihtsamaid gaasiosakesi peetakse täiuslikult elastseteks kuulideks, mis interakteeruvad nii üksteisega kui ka mis tahes anuma seinte molekulidega ainult ühel juhul - absoluutselt elastne kokkupõrge;
- gaasi sees olevad tõmbejõud puuduvad või võib neid tegelikult tähelepanuta jätta;
- gaasi sisestruktuuri elemente võib võtta kui materiaalseid punkte, st nende ruumala võib samuti tähelepanuta jätta.
Sellist mudelit silmas pidades kirjutas Saksa päritolu füüsik Rudolf Clausius gaasirõhu valemi mikro- ja makroskoopiliste parameetrite seose kaudu. See näeb välja selline:
p=1/3m(0)nv^2.
Hiljem nimetatakse seda valemit ideaalse gaasi molekulaarkineetilise teooria põhivõrrandiks. Seda saab esitada mitmel erineval kujul. Meie ülesanne on nüüd näidata selliseid jaotisi nagu molekulaarfüüsika, molekulaarkineetiline teooria ja seega ka nende täielikud võrrandid ja tüübid. Seetõttu on mõttekas kaaluda põhivalemi muid variatsioone.
Me teame, et gaasimolekulide liikumist iseloomustava keskmise energia saab leida järgmise valemi abil: E=m(0)v^2/2.
Sel juhul saame algses rõhuvalemis avaldise m(0)v^2 asendada keskmise kineetilise energiaga. Selle tulemusena on meil võimalus koostada gaaside molekulaarkineetilise teooria põhivõrrand järgmisel kujul: p=2/3nE.
Pealegi teame kõik, et avaldise m(0)n saab kirjutada kahe jagatise korrutisena:
m/NN/V=m/V=ρ.
Pärast neid manipuleerimisi saame oma ideaalse gaasi molekulaarkineetilise teooria võrrandi valemi ümber kirjutada kolmandal erineval kujul:
p=1/3ρv^2.
Noh, võib-olla on see kõik, mida peate selle teema kohta teadma. Jääb üle vaid lühikeste (ja mitte nii) järelduste vormis saadud teadmised süstematiseerida.
Kõik üldised järeldused ja valemid teemal "Molekulaarkineetiline teooria"
Nii et alustame.
Esiteks:
Füüsika on loodusteaduste hulka kuuluv fundamenta alteadus, mis uurib aine ja energia omadusi, nende struktuuri, anorgaanilise looduse mustreid.
See sisaldab järgmisi jaotisi:
- mehaanika (kinemaatika ja dünaamika);
- staatiline;
- termodünaamika;
- elektrodünaamika;
- molekulaarne sektsioon;
- optika;
- kvantide ja aatomituuma füüsika.
Teine:
Osakeste füüsika ja termodünaamika on omavahel tihed alt seotud harud, mis uurivad füüsikaliste süsteemide koguarvu eranditult makroskoopilist komponenti, st süsteeme, mis koosnevad suurest hulgast elementaarosakestest.
Need põhinevad molekulaarkineetilisel teoorial.
Kolmas:
Asja tuum on see. Molekulaarkineetiline teooria kirjeldab üksikasjalikult aine struktuuri (sagedamini gaaside kui tahkete ainete ehitust).ja vedelkehad), mis põhinevad kolmel põhieeldusel, mis koguti väljapaistvate teadlaste eeldustest. Nende hulgas: Robert Hooke, Isaac Newton, Daniel Bernoulli, Mihhail Lomonosov ja paljud teised.
Neljas:
Molekulaarkineetilise teooria kolm põhipõhimõtet:
- Kõigil ainetel (olenemata sellest, kas need on vedelad, tahked või gaasilised) on keeruline struktuur, mis koosneb väiksematest osakestest: molekulidest ja aatomitest.
- Kõik need lihtsad osakesed on pidevas kaootilises liikumises. Näide: Browni liikumine ja difusioon.
- Kõik molekulid mis tahes tingimustes interakteeruvad üksteisega teatud jõududega, millel on elektriline kivim.
Kõik need molekulaarkineetilise teooria sätted on kindla aluse aine struktuuri uurimisel.
Viies:
Mitmed molekulaarteooria põhipunktid gaasimudeli jaoks:
- Kõik gaasid koosnevad elementaarosakestest, millel ei ole teatud suurust, kuid millel on kindel mass. Teisisõnu, nende osakeste maht on nendevaheliste kaugustega võrreldes minimaalne.
- Gaasi aatomitel ja molekulidel praktiliselt puudub potentsiaalne energia, vastav alt nende koguenergia on võrdne kineetilise energiaga.
- Selle seisukohaga tutvusime juba varem - Browni liikumine. See tähendab, et gaasiosakesed on alati pidevas ja juhuslikus liikumises.
- Absoluutselt kõik aatomite ja gaasimolekulide vastastikused kokkupõrked, millega kaasneb sõnum kiirusest ja energiast, on täiesti elastsed. See ontähendab, et kokkupõrke ajal ei esine energiakadu ega järske hüppeid nende kineetilises energias.
- Norma altingimustes ja püsival temperatuuril on peaaegu kõigi gaaside keskmine kineetiline energia sama.
Kuues:
Järeldused gaaside teooriast:
- Absoluutne temperatuur on selle aatomite ja molekulide keskmise kineetilise energia mõõt.
- Kui kaks erinevat gaasi on samal temperatuuril, on nende molekulidel sama keskmine kineetiline energia.
- Gaasiosakeste keskmine kineetiline energia on otseselt võrdeline ruutkeskmise kiirusega: E=1/2mv^2.
- Kuigi gaasimolekulidel on vastav alt keskmine kineetiline energia ja keskmine kiirus, liiguvad üksikud osakesed erineva kiirusega: mõned kiiresti, mõned aeglaselt.
- Mida kõrgem on temperatuur, seda suurem on molekulide kiirus.
- Mitu korda me gaasi temperatuuri tõstame (näiteks kahekordistame), nii mitu korda suureneb (vastav alt kahekordistub) ka selle osakeste keskmine kineetiline energia.
- Seos gaasi rõhu vahel anuma seintel, milles see asub, ja molekulide nendele seintele avaldatavate mõjude intensiivsuse vahel on otseselt võrdeline: mida rohkem lööke, seda suurem on rõhk ja vastupidi.
Seitsmes:
Ideaalne gaasimudel on mudel, mille puhul peavad olema täidetud järgmised tingimused:
- Gaasi molekulid võivad ja neid peetakse ideaalselt elastseteks kuulideks.
- Need pallid võivad suhelda üksteisega ja mis tahes seintegalaev ainult ühel juhul - absoluutselt elastne kokkupõrge.
- Need jõud, mis kirjeldavad vastastikust tõukejõudu gaasi aatomite ja molekulide vahel, puuduvad või neid võib tegelikult tähelepanuta jätta.
- Aatomeid ja molekule käsitletakse materiaalsete punktidena, st nende ruumala võib samuti tähelepanuta jätta.
Kaheksas:
Anname kõik põhivõrrandid ja näitame valemeid teemas "Molekulaarkineetiline teooria":
p=1/3m(0)nv^2 - ideaalse gaasi mudeli põhivõrrand, mille on tuletanud saksa füüsik Rudolf Clausius.
p=2/3nE - ideaalse gaasi molekulaarkineetilise teooria põhivõrrand. Tuletatud molekulide keskmisest kineetilisest energiast.
р=1/3ρv^2 - sama võrrand, kuid vaadeldakse ideaalsete gaasimolekulide tiheduse ja ruutkeskmise kiiruse kaudu.
m(0)=M/N(a) - valem ühe molekuli massi leidmiseks Avogadro arvu kaudu.
v^2=(v(1)+v(2)+v(3)+…)/N - valem molekulide keskmise ruutkiiruse leidmiseks, kus v(1), v(2), v (3) ja nii edasi - esimese molekuli kiirus, teise, kolmanda ja nii edasi kuni n-nda molekulini.
n=N/V - valem molekulide kontsentratsiooni leidmiseks, kus N on molekulide arv gaasimahus antud ruumalas V.
E=mv^2/2=3/2kT - molekulide keskmise kineetilise energia leidmise valemid, kus v^2 on molekulide ruutkeskmine kiirus, k on konstant väärtus on nimetatud austerlase järgi Ludwig Boltzmanni füüsika järgi ja T on gaasi temperatuur.
p=nkT - rõhuvalem kontsentratsiooni järgi, konstantBoltzmann ja absoluutne temperatuur T. Sellest tuleneb veel üks põhivalem, mille avastasid vene teadlane Mendelejev ja prantsuse füüsik-insener Claiperon:
pV=m/MRT, kus R=kN(a) on gaaside universaalne konstant.
Nüüd näitame erinevate isoprotsesside konstandid: isobaarne, isohooriline, isotermiline ja adiabaatiline.
pV/T=const - tehakse, kui gaasi mass ja koostis on konstantsed.
рV=const - kui ka temperatuur on konstantne.
V/T=const - kui gaasirõhk on konstantne.
p/T=const - kui helitugevus on konstantne.
Võib-olla on see kõik, mida pead selle teema kohta teadma.
Täna sukeldusime sellisesse teadusvaldkonda nagu teoreetiline füüsika, selle mitmed osad ja plokid. Üksikasjalikum alt puudutasime sellist füüsika valdkonda nagu fundamentaalne molekulaarfüüsika ja termodünaamika, nimelt molekulaarkineetiline teooria, mis näib, et esialgses uuringus ei tekita raskusi, kuid millel on tegelikult palju lõkse.. See laiendab meie arusaama ideaalsest gaasimudelist, mida me ka üksikasjalikult uurisime. Lisaks väärib märkimist, et tutvusime ka molekulaarteooria põhivõrranditega nende erinevates variatsioonides ning vaagisime läbi ka kõik kõige vajalikumad valemid antud teemal teatud tundmatute suuruste leidmiseks. See tuleb eriti kasuks kirjutama valmistumisel. mis tahes testide, eksamite ja testide jaoks või üldiste väljavaadete ja füüsikateadmiste laiendamiseks.
Loodame, et see artikkel oli teile kasulik ja olete sellest ammutanud ainult kõige vajalikuma teabe, tugevdades oma teadmisi termodünaamika sellistes sammastes nagu molekulaarkineetilise teooria põhisätted.






