Termodünaamika on oluline füüsika haru. Võime julgelt väita, et selle saavutused on viinud tehnoloogiaajastu tekkeni ja suuresti määranud inimkonna ajaloo kulgemise viimase 300 aasta jooksul. Artiklis käsitletakse termodünaamika esimest, teist ja kolmandat seadust ning nende rakendamist praktikas.
Mis on termodünaamika?
Enne termodünaamika seaduste sõnastamist mõelgem välja, mida see füüsika osa teeb.
Sõna "termodünaamika" on kreeka päritolu ja tähendab "kuumusest tingitud liikumist". See tähendab, et see füüsika haru tegeleb mis tahes protsesside uurimisega, mille tulemusena soojusenergia muundub mehaaniliseks liikumiseks ja vastupidi.
Terodünaamika põhiseadused sõnastati 19. sajandi keskel. "Liikumise ja soojuse" teadus käsitleb kogu süsteemi käitumist tervikuna, uurides selle makroskoopiliste parameetrite - temperatuuri, rõhu ja mahu muutumist, mitte pöörates tähelepanu selle mikroskoopilisele struktuurile. Veelgi enam, esimene neist mängib olulist rolli seaduste sõnastamiseltermodünaamika füüsikas. Huvitav on märkida, et need on saadud ainult eksperimentaalsetest vaatlustest.
Terodünaamilise süsteemi kontseptsioon

See tähendab mis tahes aatomite, molekulide või muude elementide rühma, mida käsitletakse tervikuna. Kõik kolm seadust on sõnastatud nn termodünaamilise süsteemi jaoks. Näited on: Maa atmosfäär, mis tahes elusorganismid, gaasisegu sisepõlemismootoris jne.
Kõik termodünaamika süsteemid kuuluvad ühte kolmest tüübist:
- Avatud. Nad vahetavad keskkonnaga nii soojust kui ainet. Näiteks kui toitu keedetakse potis lahtisel tulel, siis on see avatud süsteemi ilmekas näide, kuna pott saab energiat väliskeskkonnast (tulest), ise aga kiirgab energiat soojuse kujul, ja se alt aurustub ka vesi (ainevahetus).
- Suletud. Sellistes süsteemides ei toimu ainevahetust keskkonnaga, kuigi energiavahetus toimub. Tulles tagasi eelmise juhtumi juurde: kui kata veekeetja kaanega, saad suletud süsteemi.
- Isoleeritud. See on omamoodi termodünaamiline süsteem, mis ei vaheta ümbritseva ruumiga ainet ega energiat. Näiteks võib tuua kuuma teed sisaldava termose.
Termodünaamiline temperatuur

See mõiste tähendab ümbritsevaid kehasid moodustavate osakeste kineetilist energiat, mis peegeldab kiirustosakeste juhuslik liikumine. Mida suurem see on, seda kõrgem on temperatuur. Vastav alt sellele jahutame süsteemi kineetilist energiat vähendades.
See mõiste tähendab ümbritsevaid kehasid moodustavate osakeste kineetilist energiat, mis peegeldab osakeste kaootilise liikumise kiirust. Mida suurem see on, seda kõrgem on temperatuur. Vastav alt sellele jahutame süsteemi kineetilist energiat vähendades.
Termodünaamilist temperatuuri väljendatakse SI-s (rahvusvaheline ühikute süsteem) kelvinites (Briti teadlase William Kelvini auks, kes selle skaala esmakordselt pakkus). Termodünaamika esimese, teise ja kolmanda seaduse mõistmine on võimatu ilma temperatuuri määratluseta.
Ühe kraadi jaotus Kelvini skaalal vastab ka ühele Celsiuse kraadile. Nende ühikute teisendamine toimub järgmise valemi järgi: TK =TC + 273, 15, kus TK ja TC - temperatuurid vastav alt kelvinites ja Celsiuse kraadides.
Kelvini skaala eripära on see, et sellel puuduvad negatiivsed väärtused. Null selles (TC=-273, 15 oC) vastab olekule, mil süsteemi osakeste soojusliikumine puudub täielikult, näivad need olevat "külmutatud".
Energia jäävus ja termodünaamika 1. seadus

Aastal 1824 tegi prantsuse insener ja füüsik Nicolas Léonard Sadi Carnot julge ettepaneku, mis mitte ainult ei viinud füüsika arenguni, vaid sai ka oluliseks sammuks tehnoloogia täiustamisel. Temavõib sõnastada järgmiselt: "Energiat ei saa luua ega hävitada, seda saab ainult ühest olekust teise üle kanda."
Tegelikult postuleerib Sadi Carnot' fraas energia jäävuse seadust, mis oli termodünaamika 1. seaduse aluseks: "Kui süsteem saab energiat väljastpoolt, muundab see selle muudeks vormideks, mis on termilised ja mehaanilised."
1. seaduse matemaatiline valem on kirjutatud järgmiselt:
Q=ΔU + A, siin Q on keskkonna poolt süsteemile ülekantav soojushulk, ΔU on selle süsteemi siseenergia muutus, A on täiuslik mehaaniline töö.
Adiabaatilised protsessid
Hea näide neist on õhumasside liikumine mööda mäenõlvu. Sellised massid on tohutud (kilomeetrid või rohkem) ja õhk on suurepärane soojusisolaator. Märgitud omadused võimaldavad meil pidada adiabaatilisteks kõiki õhumassidega protsesse, mis toimuvad lühikese aja jooksul. Kui õhk tõuseb mäenõlvast üles, siis selle rõhk langeb, see paisub, st teeb mehaanilist tööd ja selle tulemusena jahtub. Vastupidi, õhumassi allapoole liikumisega kaasneb rõhu tõus selles, see surub kokku ja muutub seetõttu väga kuumaks.
Eelmises alapealkirjas käsitletud termodünaamika seaduse rakendamist on kõige lihtsam demonstreerida adiabaatilise protsessi näitel.
Definitsiooni kohaselt ei toimu selle tulemusena energiavahetustkeskkond, st ül altoodud võrrandis on Q=0. See toob kaasa järgmise avaldise: ΔU=-A. Miinusmärk tähendab siin seda, et süsteem teeb mehaanilist tööd, vähendades oma sisemist energiat. Tuleb meeles pidada, et siseenergia sõltub otseselt süsteemi temperatuurist.
Soojusprotsesside suund
See number käsitleb termodünaamika 2. seadust. Kindlasti märkasid kõik, et kui puutute kokku kaks erineva temperatuuriga eset, siis külm soojeneb alati ja kuum jahtub. Pange tähele, et pöördprotsess võib toimuda termodünaamika esimese seaduse raames, kuid seda ei rakendata kunagi praktikas.
Selle protsessi (ja kõigi universumis teadaolevate protsesside) pöördumatuse põhjuseks on süsteemi üleminek tõenäolisemasse olekusse. Vaadeldavas näites kahe erineva temperatuuriga keha kokkupuutel on kõige tõenäolisem olek, kus süsteemi kõikidel osakestel on sama kineetiline energia.
Termodünaamika teise seaduse võib sõnastada järgmiselt: "Kuumus ei saa kunagi külm alt keh alt iseeneslikult üle kanda kuumale." Kui tutvustame entroopia mõistet kui häire mõõdet, siis saab seda esitada järgmiselt: "Iga termodünaamiline protsess kulgeb koos entroopia suurenemisega".
Soojusmootor

Selle mõiste all mõistetakse süsteemi, mis välise energiaga varustamise tõttu suudab teha mehaanilisi töid. Esitekssoojusmasinad olid aurumasinad ja leiutati 17. sajandi lõpus.
Termodünaamika teine seadus mängib nende tõhususe määramisel otsustavat rolli. Sadi Carnot tegi ka kindlaks, et selle seadme maksimaalne efektiivsus on: Tõhusus=(T2 - T1)/T2, siin T2 ja T1 on küttekeha ja külmiku temperatuurid. Mehaanilist tööd saab teha ainult siis, kui kuumus liigub kuum alt keh alt külma ja seda voolu ei saa 100% muuta kasulikuks energiaks.
Allpool olev joonis näitab soojusmasina tööpõhimõtet (Qabs - masinale üle kantud soojus, Qced - soojuskadu, W - kasulik töö, P ja V - rõhk ja gaasi maht kolvis).
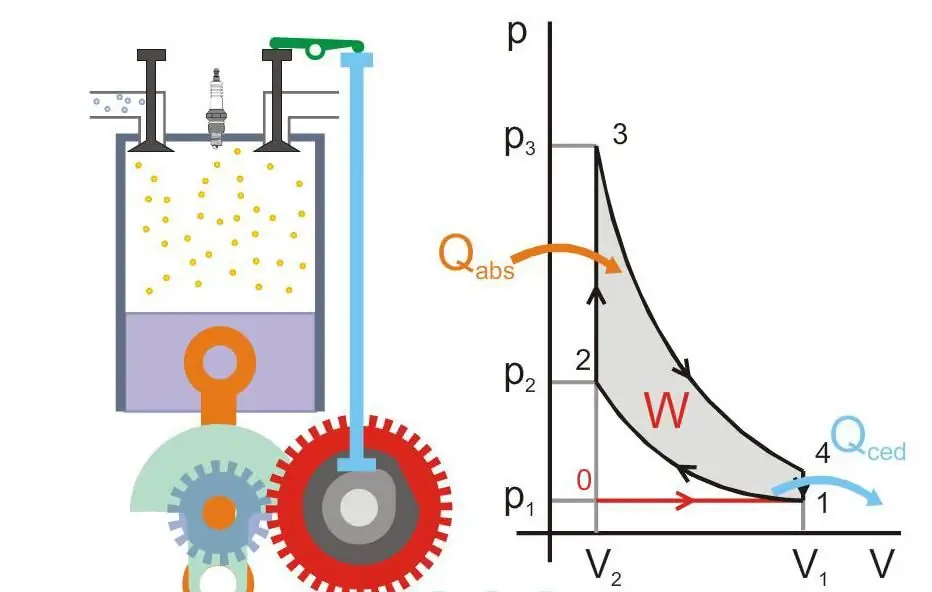
Absoluutne null ja Nernsti postulaat
Lõpuks liigume edasi termodünaamika kolmanda seaduse käsitlemise juurde. Seda nimetatakse ka Nernsti postulaadiks (20. sajandi alguses selle esimest korda sõnastanud saksa füüsiku nimi). Seadus ütleb: "Absoluutset nulli ei saa saavutada piiratud arvu protsessidega." See tähendab, et aine molekule ja aatomeid pole mingil viisil võimalik täielikult "külmutada". Selle põhjuseks on pidev olemasolev soojusvahetus keskkonnaga.

Üks kasulik järeldus termodünaamika kolmandast seadusest on see, et entroopia väheneb absoluutse nulli poole liikudes. See tähendab, et süsteem kipub end organiseerima. See asjaolu võibkasutada näiteks paramagnetite jahutamisel ferromagnetilisse olekusse viimiseks.
Huvitav on märkida, et seni saavutatud madalaim temperatuur on 5·10−10 K (2003, MIT labor, USA).






