Meie ajal on füüsikast saanud väga levinud teadus. See on sõna otseses mõttes kõikjal olemas. Kõige elementaarsem näide: sinu õues kasvab õunapuu ja sellel valmivad viljad, tuleb aeg ja õunad hakkavad langema, aga mis suunas kukuvad? Tänu universaalse gravitatsiooni seadusele kukub meie loode maapinnale ehk laskub alla, aga mitte üles. See oli üks kuulsamaid füüsika näiteid, kuid pöörakem tähelepanu termodünaamikale või täpsem alt faasitasakaaludele, mis pole meie elus vähem tähtsad.
Termodünaamika

Kõigepe alt vaatame seda terminit. ΘερΜοδυναΜική - nii näeb see sõna kreeka keeles välja. Esimene osa ΘερΜo tähendab "soojust" ja teine δυναΜική tähendab "jõudu". Termodünaamika on füüsika haru, mis uurib makroskoopilise süsteemi omadusi, aga ka erinevaid energia muundamise ja ülekandmise viise. Selles jaotises uuritakse spetsiaalselt erinevaid olekuid ja protsesse, et kirjeldusse saaks sisse viia temperatuuri mõiste (see on füüsikaline suurus, mis iseloomustab termodünaamilist süsteemi ja mida mõõdetakseteatud seadmed). Kõiki termodünaamilistes süsteemides toimuvaid protsesse kirjeldatakse ainult mikroskoopiliste suurustega (rõhk ja temperatuur, samuti komponentide kontsentratsioon).
Clapeyroni-Clausiuse võrrand
Iga füüsik teab seda võrrandit, kuid jagame selle osade kaupa lahti. See viitab tasakaaluprotsessidele teatud aine üleminekul ühest faasist teise. Seda on selgelt näha sellistes näidetes: sulamine, aurustamine, sublimatsioon (üks toodete säilitamise viise, mis toimub niiskuse täieliku eemaldamise teel). Valem näitab selgelt käimasolevaid protsesse:
- n=PV/RT;
- kus T on aine temperatuur;
- P-rõhk;
- R-spetsiifiline faasisiirdesoojus;
- V-muutus konkreetses helitugevuses.
Võrrandi loomise ajalugu

Clausiuse-Clapeyroni võrrand on termodünaamika teise seaduse suurepärane matemaatiline seletus. Seda nimetatakse ka "Clausiuse ebavõrdsuseks". Loomulikult töötas teoreemi välja teadlane ise, kes soovis selgitada süsteemi soojusvoo ja entroopia ning selle keskkonna vahelist seost. Selle võrrandi töötas välja Clausius, püüdes selgitada ja kvantifitseerida entroopiat. Otseses mõttes annab teoreem meile võimaluse määrata, kas tsükliline protsess on pöörduv või pöördumatu. See ebavõrdsus pakub meile teise seaduse mõistmiseks kvantitatiivse valemi.
Teadlane oli üks esimesi, kes töötas entroopia idee kallal ja isegi andis selleprotsessi nimi. See, mida praegu tuntakse Clausiuse teoreemina, avaldati esmakordselt 1862. aastal Rudolfi kuuendas teoses „Teisenduste ekvivalentsusteoreemi kasutamine sisetöös”. Teadlane püüdis näidata proportsionaalset seost entroopia ja energiavoo vahel süsteemi kuumutamise (δ Q) abil. Ehituses saab selle soojusenergia muundada tööks ja tsüklilise protsessi kaudu soojuseks. Rudolph tõestas, et "kõigi tsüklilises protsessis toimuvate teisenduste algebraline summa võib olla väiksem kui null või äärmuslikel juhtudel võrdne nulliga."
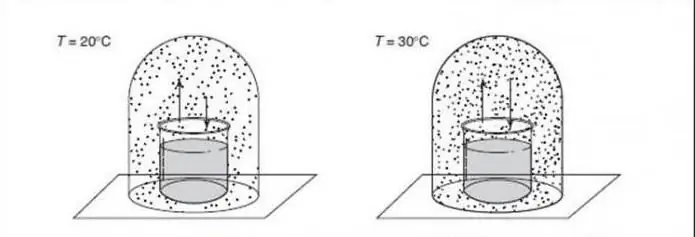
Suletud isoleeritud süsteem
Isoleeritud süsteem on üks järgmistest:
- Füüsiline süsteem on kaugel teistest, kes nendega ei suhtle.
- Terodünaamiline süsteem on suletud jäikade liikumatute seintega, millest ei pääse läbi ei aine ega energia.
Hoolimata asjaolust, et objekt on sisemiselt seotud oma gravitatsiooniga, viiakse isoleeritud süsteem tavaliselt väljapoole väliste gravitatsiooni- ja muude kaugete jõudude piire.
Seda võib vastandada sellele, mida (termodünaamikas kasutatava üldisema terminoloogia järgi) nimetatakse suletud süsteemiks, mida ümbritsevad selektiivsed seinad, mille kaudu saab soojuse või töö kujul üle kanda energiat, kuid mitte ainet. Ja avatud süsteemiga, milles aine ja energia sisenevad või väljuvad, kuigi sellel võivad olla erinevad läbitungimatud seinadosa selle piiridest.
Isoleeritud süsteem järgib looduskaitseseadust. Kõige sagedamini käsitletakse termodünaamikas ainet ja energiat eraldi mõistetena.
Termodünaamilised üleminekud
Kvantfaasisiiretest arusaamiseks on kasulik neid võrrelda klassikaliste teisendustega (nimetatakse ka termilisteks inversioonideks). CPT kirjeldab süsteemi termodünaamiliste omaduste tippu. See annab märku osakeste ümberkorraldamisest. Tüüpiline näide on vee jäätumisüleminek, mis kirjeldab sujuvat üleminekut vedeliku ja tahke aine vahel. Klassikaline faasikasv on tingitud konkurentsist süsteemi energia ja selle termiliste kõikumiste entroopia vahel.
Klassikalisel süsteemil puudub nulltemperatuuril entroopia ja seetõttu ei saa toimuda faasimuutust. Nende järjestuse määrab esimene katkendlik tuletistermodünaamiline potentsiaal. Ja loomulikult on sellel esimene järjekord. Faaside teisendused ferromagnetist paramagnetiks on pidevad ja teist järku. Neid pidevaid muutusi järjestatud faasist korrastamata faasini kirjeldatakse järjestusparameetriga, mis on null. Ül altoodud ferromagnetilise teisenduse korral on järjestusparameetriks süsteemi kogumagnetiseeritus.
Gibbsi potentsiaal
The Gibbs Free Energy on maksimaalne töömaht ilma paisuta, mida saab eemaldada termodünaamilise suletud süsteemiga (mis suudab soojust vahetada ja töötada koos keskkonnaga). Sellisedmaksimaalse tulemuse saab ainult täiesti pöörduva protsessiga. Kui süsteem muundub tagasi esimesest olekust teise, on Gibbsi vaba energia vähenemine võrdne süsteemi poolt keskkonnas saavutatavaga, millest on maha arvatud survejõudude töö.
Tasakaaluseisud

Termodünaamiline ja mehaaniline tasakaal on termodünaamika aksiomaatiline mõiste. See on ühe või mitme süsteemi sisemine olek, mis on ühendatud enam-vähem läbilaskvate või mitteläbilaskvate seintega. Selles olekus ei toimu puhtaid makroskoopilisi aine- ega energiavooge ei süsteemi sees ega süsteemide vahel.
Sisemise tasakaaluseisundi enda arusaama järgi makroskoopilisi muutusi ei toimu. Süsteemid on samaaegselt vastastikuses termilises, mehaanilises, keemilises (konstantses), kiirguse tasakaalus. Need võivad olla samal kujul. Selle protsessi käigus salvestatakse kõik vaated korraga ja määramata ajaks, kuni füüsiline toiming katkeb. Makroskoopilises tasakaalus toimuvad täiesti täpsed tasakaalustatud vahetused. Ül altoodud tõend on selle kontseptsiooni füüsiline seletus.
Põhitõed
Igal seadusel, teoreemil, valemil on oma alused. Vaatame faasitasakaalu seaduse kolme alust.
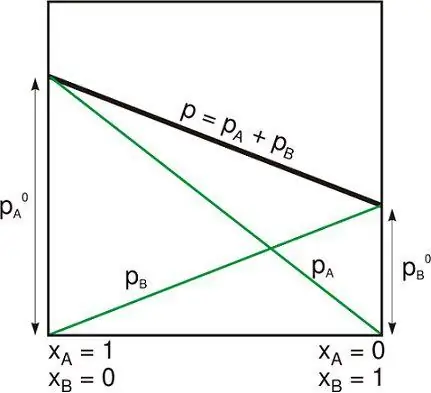
- Faas on aine vorm, mis on keemilise koostise, füüsikalise oleku ja mehaanilise tasakaalu poolest homogeenne. Tüüpilised faasid on tahked, vedelad ja gaasilised. Kahte eraldi piiriga eraldatud segunematut vedelikku (või erineva koostisega vedelat segu) loetakse kaheks erinevaks faasiks ja segunematuks tahkeks aineks.
- Komponentide arv (C) on süsteemi keemiliselt sõltumatute komponentide arv. Minimaalne sõltumatute liikide arv, mis on vajalik süsteemi kõigi faaside koostise määramiseks.
- Vabadusastmete arv (F) on selles kontekstis üksteisest sõltumatute intensiivsete muutujate arv.
Klassifikatsioon faasitasakaalu järgi
- Pideva netoülekande reaktsioonid (mida sageli nimetatakse tahkisreaktsioonideks) toimuvad erineva koostisega tahkete ainete vahel. Need võivad sisaldada vedelikes leiduvaid elemente (H, C), kuid need elemendid säilivad tahketes faasides, seega ei ole vedelad faasid reaktiividena ega toodetena kaasatud (H2O, CO2). Tahkete puhaste ülekandereaktsioonid võivad olla pidevad või katkendlikud või lõplikud.
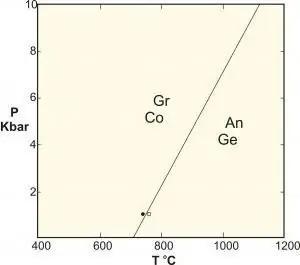
- Polümorfsed on tahkefaasiliste reaktsioonide eritüüp, mis hõlmab identse koostisega faase. Klassikalised näited on reaktsioonid alumiiniumsilikaatide küaniidi-sillimaniidi-andalusiidi vahel, grafiidi muundamine teemandiks kõrgel rõhul ja k altsiumkarbonaadi tasakaal.
Tasakaaluseadused

Gibbsi tehase reegli pakkus välja Josiah Willard Gibbs oma kuulsas artiklis "The Equilibrium of Heterogeneous Substances", mis ilmus aastatel 1875-1878. See kehtibmittereaktiivsed mitmekomponendilised heterogeensed süsteemid termodünaamilises tasakaalus ja on antud võrdsus:
- F=C-P+2;
- kus F on vabadusastmete arv;
- C - komponentide arv;
- P - üksteisega termodünaamilises tasakaalus olevate faaside arv.
Vabadusastmete arv on hõivamata intensiivsete muutujate arv. Suurim arv termodünaamilisi parameetreid, nagu temperatuur või rõhk, mis võivad muutuda samaaegselt ja suvaliselt ilma üksteist mõjutamata. Ühekomponendilise süsteemi näide on see, mis sisaldab ühte puhast kemikaali, samas kui kahekomponentsetel süsteemidel, nagu vee ja etanooli segud, on kaks sõltumatut komponenti. Tüüpilised faasisiirded (faasitasakaal) on tahked ained, vedelikud, gaasid.
Faasireegel konstantsel rõhul
Materjaliteaduse rakenduste puhul, mis käsitlevad faasimuutusi erinevate tahkete struktuuride vahel, tekib sageli konstantne rõhk (nt üks atmosfäär) ja seda eiratakse vabadusastmena, seega muutub reegel: F=C - P + 1.
Seda valemit kasutatakse mõnikord "kondenseeritud faasi reegli" nime all, kuid nagu me teame, ei ole see rakendatav kõrge rõhu all olevate süsteemide puhul (näiteks geoloogias), kuna nende tagajärjed on surve võib põhjustada katastroofilisi tagajärgi.
Võib tunduda, et faasitasakaal on vaid tühi fraas ja vähesed füüsilised protsessid, milles see hetkon kaasatud, kuid nagu nägime, ilma selleta ei tööta paljud meile teadaolevad seadused, seega peate tutvuma nende ainulaadsete, värvikate, kuigi pisut igavate reeglitega. Need teadmised on aidanud paljusid inimesi. Nad õppisid, kuidas neid enda puhul rakendada, näiteks saavad elektrikud, teades faasidega töötamise reegleid, end tarbetu ohu eest kaitsta.

