Gaasi soojusmahtuvus on energia hulk, mille keha neelab, kui seda kuumutatakse ühe kraadi võrra. Analüüsime selle füüsikalise suuruse põhiomadusi.

Definitsioonid
Gaasi erisoojus on konkreetse aine massiühik. Selle mõõtühikud on J/(kg·K). Soojushulk, mida keha neelab oma agregatsiooniseisundi muutmise protsessis, ei ole seotud mitte ainult alg- ja lõppolekuga, vaid ka üleminekumeetodiga.

Osakond
Gaaside soojusmahtuvus jagatakse konstantse mahu (Cv), konstantse rõhu (Cр) väärtusega.
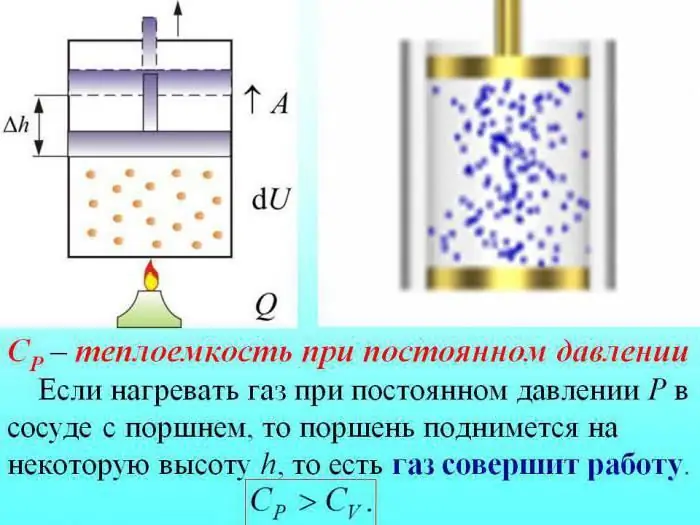
Rõhku muutmata kütmisel kulub osa soojusest gaasi paisumise tekitamiseks ja osa energiast siseenergia suurendamiseks.
Gaaside soojusmahtuvuse konstantsel rõhul määrab soojushulk, mis kulub siseenergia suurendamiseks.
Gaasi olek: omadused, kirjeldus
Ideaalse gaasi soojusmahtuvuse määramisel võetakse arvesse asjaolu, et Сp-Сv=R. Viimast suurust nimetatakse universaalseks gaasikonstandiks. Selle väärtus vastab 8,314 J/(mol K).
Soojusmahtuvuse teoreetiliste arvutuste tegemisel, näiteks temperatuuriga seose kirjeldamisel, ei piisa ainult termodünaamiliste meetodite kasutamisest, oluline on end relvastada staatilise füüsika elementidega.
Gaaside soojusmahtuvus hõlmab mõne molekuli translatsioonilise liikumise energia keskmise väärtuse arvutamist. Selline liikumine on kokku võetud molekuli pöörlevast ja translatsioonilisest liikumisest, samuti aatomite sisemisest vibratsioonist.
Staatilises füüsikas on teavet selle kohta, et iga pöörleva ja translatsioonilise liikumise vabadusastme jaoks on gaasi kogus, mis on võrdne poolega universaalsest gaasikonstandist.

Huvitavaid fakte
Eeldatakse, et üheaatomilise gaasi osakesel on kolm translatsioonivabadusastet, seega on gaasi erisoojusel kolm translatsiooni-, kaks pöörlemis- ja üks vibratsioonivabadusastet. Nende ühtlase jaotuse seadus viib konstantse ruumala juures erisoojuse võrdsustamiseni R.
Katsete käigus selgus, et kaheaatomilise gaasi soojusmahtuvus vastab väärtusele R. Sellist lahknevust teooria ja praktika vahel seletab asjaolu, et ideaalse gaasi soojusmahtuvus on seotud kvantiga mõjusid, seetõttu on arvutuste tegemisel oluline kasutada kvantipõhist statistikatmehaanika.
Kvantmehaanika alustele tuginedes on mis tahes võnkuvatel või pöörlevatel osakeste süsteemil, sealhulgas gaasimolekulidel, vaid mõned diskreetsed energiaväärtused.
Kui süsteemi soojusliikumise energiast ei piisa teatud sagedusega võnkumiste tekitamiseks, ei aita sellised liikumised kaasa süsteemi kogu soojusmahtuvusele.
Selle tulemusena "külmub" konkreetne vabadusaste, sellele on võimatu rakendada võrdsusseadust.
Gaasi soojusmahtuvus on oleku oluline tunnus, millest sõltub kogu termodünaamilise süsteemi toimimine.
Temperatuuri, mille juures saab võrdsusseadust rakendada võnke- või pöörlemisvabadusastmele, iseloomustab kvantteooria, see ühendab Plancki konstandi Boltzmanni konstandiga.

Diatomilised gaasid
Selliste gaaside pöörlemisenergia tasemete vahe on väike arv kraadi. Erandiks on vesinik, mille temperatuuri väärtus määratakse sadade kraadidega.
Seetõttu on gaasi soojusmahtuvust konstantsel rõhul raske ühtlase jaotuse seadusega kirjeldada. Kvantstatistikas võetakse soojusmahtuvuse määramisel arvesse, et selle vibratsiooniline osa temperatuuri languse korral kiiresti väheneb ja jõuab nullini.
See nähtus seletab asjaolu, et toatemperatuuril puudub soojusmahtuvuse vibratsiooniline osa,kaheaatomiline gaas, see vastab konstandile R.
Gaasi soojusmahtuvus konstantse mahu juures madala temperatuuri indikaatorite korral määratakse kvantstatistika abil. On olemas Nernsti printsiip, mida nimetatakse termodünaamika kolmandaks seaduseks. Selle koostise põhjal väheneb gaasi molaarne soojusmahtuvus temperatuuri langedes, kaldudes nullini.

Tahkeainete omadused
Kui gaasisegu soojusmahtuvust saab selgitada kvantstatistika abil, siis agregatsiooni tahkes olekus iseloomustab soojusliikumist osakeste kerge kõikumine tasakaaluasendi lähedal.
Igal aatomil on kolm võnkevabadusastet, seetõttu saab vastav alt võrdse jaotusseadusele arvutada tahke aine molaarse soojusmahtuvuse väärtuseks 3nR, kusjuures n on aatomite arv molekulis.
Praktikas on see arv piir, milleni tahke keha soojusmahtuvus kõrgel temperatuuril kipub.
Mõnede elementide, sealhulgas metallide puhul võib maksimumi saada tavatemperatuuril. N=1 puhul on Dulongi ja Petiti seadus täidetud, kuid kompleksainete puhul on sellise piirini üsna raske jõuda. Kuna tegelikkuses piiri ei ole võimalik saada, toimub tahke aine lagunemine või sulamine.
Kvantteooria ajalugu
Kvantteooria rajajad on Einstein ja Debye kahekümnenda sajandi alguses. See põhineb aatomite võnkuvate liikumiste kvantiseerimisel teatud kindlas kohaskristall. Madalate temperatuurinäitajate puhul osutub tahke keha soojusmahtuvus otseselt võrdeliseks kuubiks võetud absoluutväärtusega. Seda suhet on nimetatud Debye seaduseks. Kriteeriumina, mis võimaldab eristada madala ja kõrge temperatuuri indikaatoreid, võetakse nende võrdlus Debye'i temperatuuriga.
Selle väärtuse määrab kehas oleva aatomi vibratsioonispekter, seega sõltub see tõsiselt selle kristallstruktuuri omadustest.
QD on väärtus, millel on mitusada K, kuid näiteks teemandis on see palju suurem.
Juhtivuselektronid annavad olulise panuse metallide soojusmahtuvusse. Selle arvutamiseks kasutatakse Fermi kvantstatistikat. Metalli aatomite elektrooniline juhtivus on otseselt võrdeline absoluutse temperatuuriga. Kuna see on ebaoluline väärtus, võetakse seda arvesse ainult absoluutse nulli poole kalduvatel temperatuuridel.
Soojusmahtuvuse määramise meetodid
Peamine katsemeetod on kalorimeetria. Soojusmahtuvuse teoreetiliseks arvutamiseks kasutatakse statistilist termodünaamikat. See kehtib nii ideaalse gaasi kui ka kristalsete kehade kohta, tehakse aine struktuuri eksperimentaalsete andmete põhjal.
Ideaalse gaasi soojusmahtuvuse arvutamise empiirilised meetodid põhinevad ideel keemilisest struktuurist, üksikute aatomirühmade panusest Ср.
Vedelate puhul kasutatakse ka meetodeid, mis põhinevad termodünaamika kasutamiseltsüklid, mis võimaldavad ideaalse gaasi soojusmahtuvuselt aurustumisprotsessi entalpia temperatuuri tuletise kaudu vedelikku üle minna.
Lahenduse puhul ei ole soojusmahtuvuse arvutamine liitfunktsioonina lubatud, kuna lahuse soojusmahtuvuse liigväärtus on põhimõtteliselt oluline.
Selle hindamiseks vajame lahenduste molekulaarstatistilist teooriat. Kõige keerulisem on heterogeensete süsteemide soojusmahtuvuse tuvastamine termodünaamilises analüüsis.

Järeldus
Soojusmahtuvuse uuring võimaldab arvutada keemiareaktorites, aga ka teistes keemiatootmisseadmetes toimuvate protsesside energiabilanssi. Lisaks on see väärtus vajalik optimaalsete jahutusvedelike tüüpide valimiseks.
Praegu on aine termodünaamiliste omaduste määramise peamine võimalus ainete soojusmahtuvuse eksperimentaalne määramine erinevatel temperatuurivahemikel - madalatest väärtustest kõrgete väärtusteni. Aine entroopia ja entalpia arvutamisel kasutatakse soojusmahtuvuse integraale. Teave keemiliste reaktiivide soojusmahtuvuse kohta teatud temperatuurivahemikus võimaldab arvutada protsessi termilise efekti. Teave lahenduste soojusmahtuvuse kohta võimaldab arvutada nende termodünaamilisi parameetreid mis tahes temperatuuri väärtustel analüüsitud intervalli piires.
Näiteks vedelikku iseloomustab see, et osa soojusest kulub potentsiaalse energia väärtuse muutmiseksreageerivad molekulid. Seda väärtust nimetatakse "konfiguratsiooni" soojusvõimsuseks, mida kasutatakse lahenduste kirjeldamiseks.
Raske on teha täiemahulisi matemaatilisi arvutusi, võtmata arvesse aine termodünaamilisi omadusi, selle agregatsiooni olekut. Seetõttu kasutatakse vedelike, gaaside, tahkete ainete puhul sellist omadust nagu erisoojusmahtuvus, mis võimaldab iseloomustada aine energiaparameetreid.






