Meid ümbritsevad loodusnähtused ja protsessid on üsna keerulised. Nende täpseks füüsikaliseks kirjeldamiseks tuleks kasutada kohmakat matemaatilist aparaati ja arvestada tuleks paljude oluliste teguritega. Selle probleemi vältimiseks kasutatakse füüsikas mõningaid lihtsustatud mudeleid, mis hõlbustavad oluliselt protsessi matemaatilist analüüsi, kuid praktiliselt ei mõjuta selle kirjelduse täpsust. Üks neist on ideaalne gaasimudel. Vaatleme seda artiklis üksikasjalikum alt.
Ideaalse gaasi kontseptsioon
Ideaalne gaas on aine agregatsiooni olek, mis koosneb materiaalsetest punktidest, mis ei interakteeru üksteisega. Selgitagem seda määratlust üksikasjalikum alt.
Esiteks räägime materiaalsetest punktidest kui objektidest, mis moodustavad ideaalse gaasi. See tähendab, et selle molekulidel ja aatomitel ei ole suurust, vaid neil on teatud mass. See on julgeligikaudse hinnangu saab teha, võttes arvesse tõsiasja, et kõigis tegelikes gaasides madalal rõhul ja kõrgel temperatuuril on molekulide vaheline kaugus palju suurem kui nende lineaarsed mõõtmed.
Teiseks ei tohiks ideaalses gaasis olevad molekulid üksteisega suhelda. Tegelikkuses on sellised vastasmõjud alati olemas. Seega kogevad isegi väärisgaaside aatomid dipool-dipool-tõmmet. Teisisõnu on olemas van der Waalsi interaktsioonid. Võrreldes molekulide pöörlemise ja translatsioonilise liikumise kineetilise energiaga on need vastasmõjud aga nii väikesed, et ei mõjuta gaaside omadusi. Seetõttu ei saa neid praktiliste probleemide lahendamisel arvesse võtta.
Oluline on märkida, et mitte kõiki gaase, mille tihedus on madal ja temperatuur kõrge, ei saa pidada ideaalseteks. Lisaks van der Waalsi interaktsioonidele on ka teisi tugevamaid sidemeid, näiteks vesiniksidemed H2O molekulide vahel, mis põhjustavad gaasi idea altingimuste jämedat rikkumist. Sel põhjusel ei ole veeaur ideaalne gaas, kuid õhk on küll.
Ideaalse gaasi füüsiline mudel
Seda mudelit saab esitada järgmiselt: oletame, et gaasisüsteem sisaldab N osakest. Need võivad olla erinevate kemikaalide ja elementide aatomid ja molekulid. N osakeste arv on suur, seetõttu kasutatakse selle kirjeldamiseks tavaliselt ühikut "mool" (1 mool vastab Avogadro arvule). Nad kõik liiguvad mingis mahus V. Osakeste liikumisedon kaootilised ja üksteisest sõltumatud. Igal neist on teatud kiirus v ja see liigub mööda sirget rada.
Teoreetiliselt on osakeste vahelise kokkupõrke tõenäosus peaaegu null, kuna nende suurus on osakestevaheliste kaugustega võrreldes väike. Kui aga selline kokkupõrge toimub, siis on see absoluutselt elastne. Viimasel juhul säilib osakeste koguimpulss ja nende kineetiline energia.
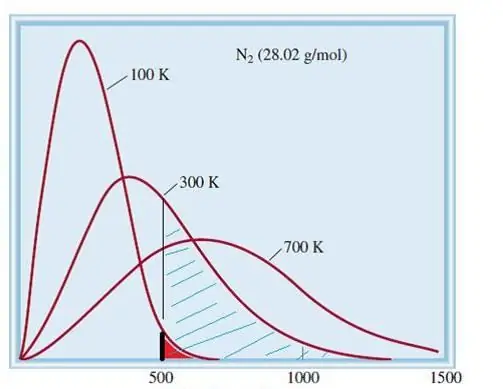
Ideaalsete gaaside vaadeldav mudel on klassikaline süsteem, millel on tohutult palju elemente. Seetõttu järgivad selles olevate osakeste kiirus ja energia Maxwell-Boltzmanni statistilist jaotust. Mõnedel osakestel on väike kiirus, teistel aga suur kiirus. Sel juhul on teatud kitsas kiiruspiirang, milles selle suuruse kõige tõenäolisemad väärtused asuvad. Lämmastiku molekulide kiirusjaotus on skemaatiliselt näidatud allpool.
Gaasi kineetiline teooria
Eelpool kirjeldatud ideaalsete gaaside mudel määrab gaaside omadused üheselt kindlaks. Selle mudeli pakkus esmakordselt välja Daniel Bernoulli aastal 1738.

Seejärel arendasid selle praeguse seisuga välja August Kroenig, Rudolf Clausius, Mihhail Lomonosov, James Maxwell, Ludwig Boltzmann, Marian Smoluchowski ja teised teadlased.
Vedelate ainete kineetiline teooria, mille põhjal ideaalse gaasi mudel ehitatakse, selgitab süsteemi kaht olulist makroskoopilist omadust selle mikroskoopilise käitumise põhjal:
- Gaasi rõhk tuleneb osakeste kokkupõrkest anuma seintega.
- Süsteemi temperatuur on molekulide ja aatomite pideva liikumise tagajärg.
Laiendame mõlemat kineetilise teooria järeldust.
Gaasirõhk
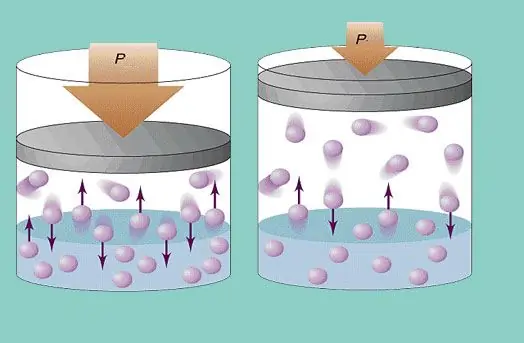
Ideaalne gaasimudel eeldab osakeste pidevat kaootilist liikumist süsteemis ja nende pidevat kokkupõrget anuma seintega. Iga sellist kokkupõrget peetakse absoluutselt elastseks. Osakeste mass on väike (≈10-27-10-25 kg). Seetõttu ei saa see kokkupõrke korral tekitada suurt survet. Sellest hoolimata on osakeste arv ja seega ka kokkupõrgete arv tohutu (≈1023). Lisaks on elementide ruutkeskmine kiirus toatemperatuuril mitusada meetrit sekundis. Kõik see viib anuma seintele märgatava surve tekkimiseni. Seda saab arvutada järgmise valemi abil:
P=Nmvcp2 / (3V), kus vcp on ruutkeskmine kiirus, m on osakese mass.
Absoluutne temperatuur
Ideaalse gaasimudeli järgi määrab temperatuuri üheselt uuritavas süsteemis molekuli või aatomi keskmine kineetiline energia. Võite kirjutada järgmise avaldise, mis seob ideaalse gaasi kineetilise energia ja absoluutse temperatuuri:
mvcp2 / 2=3/2kB T.
Siin kB on Boltzmanni konstant. Sellest võrdsusest saame:
T=m vcp2 / (3kB).
Universaalne olekuvõrrand
Kui kombineerime ül altoodud avaldised absoluutse rõhu P ja absoluutse temperatuuri T jaoks, saame kirjutada järgmise võrrandi:
PV=nRT.
Siin on n aine kogus moolides, R on D. I. Mendelejevi poolt kasutusele võetud gaasikonstant. See avaldis on ideaalsete gaaside teoorias kõige olulisem võrrand, kuna see ühendab kolm termodünaamilist parameetrit (V, P, T) ja ei sõltu gaasisüsteemi keemilistest omadustest.

Universaalvõrrandi tuletas esmakordselt eksperimentaalselt 19. sajandil prantsuse füüsik Emile Clapeyron ja seejärel viis selle tänapäevasele kujule vene keemik Mendelejev, mistõttu kannab see praegu nende teadlaste nimesid.






