Ideaalgaas, ideaalgaasi olekuvõrrand, selle temperatuur ja rõhk, maht… vastavas füüsikaosas kasutatud parameetrite ja definitsioonide loetelu võib jätkata päris pik alt. Täna räägime just sellel teemal.
Mida peetakse molekulaarfüüsikas?

Selles jaotises käsitletav põhiobjekt on ideaalne gaas. Ideaalse gaasi olekuvõrrand saadi normaalseid keskkonnatingimusi arvesse võttes ja sellest räägime veidi hiljem. Nüüd läheneme sellele "probleemile" kaugelt.
Oletame, et meil on mingi mass gaasi. Selle olekut saab määrata kolme termodünaamilise iseloomuga parameetri abil. Need on loomulikult rõhk, maht ja temperatuur. Süsteemi oleku võrrand on sel juhul vastavate parameetrite vahelise seose valem. See näeb välja selline: F (p, V, T)=0.
Siin oleme esimest korda aeglaselt lähenemas sellise asja nagu ideaal tekkimiselegaas. Seda nimetatakse gaasiks, milles molekulide vahelised vastasmõjud on tühised. Üldiselt seda looduses ei eksisteeri. Siiski on iga väga haruldane gaas sellele lähedal. Lämmastik, hapnik ja õhk, mis on normaalsetes tingimustes, erinevad ideaalist vähe. Ideaalse gaasi olekuvõrrandi kirjutamiseks saame kasutada ühtset gaasiseadust. Saame: pV/T=konst.
Seotud kontseptsioon nr 1: Avogadro seadus
Ta võib meile öelda, et kui me võtame sama arvu mooli absoluutselt suvalist gaasi ja asetame need samadesse tingimustesse, sealhulgas temperatuuri ja rõhku, siis hõivavad gaasid sama mahu. Eelkõige viidi katse läbi tavatingimustes. See tähendab, et temperatuur oli 273,15 Kelvinit, rõhk oli üks atmosfäär (760 millimeetrit elavhõbedat ehk 101325 Pascalit). Nende parameetritega hõivas gaas 22,4 liitrit. Seetõttu võime öelda, et mis tahes gaasi ühe mooli puhul on arvparameetrite suhe konstantne väärtus. Seetõttu otsustati see arv tähistada tähega R ja nimetada seda universaalseks gaasikonstandiks. Seega on see 8,31. Ühik on J/molK.
Ideaalne gaas. Ideaalse gaasi olekuvõrrand ja selle manipuleerimine
Proovime valemit ümber kirjutada. Selleks kirjutame selle järgmisel kujul: pV=RT. Järgmisena sooritame lihtsa toimingu, korrutame võrrandi mõlemad pooled suvalise arvu moolidega. Saame pVu=uRT. Võtkem arvesse asjaolu, et molaarmahu korrutis jaaine hulk on lihts alt maht. Kuid lõppude lõpuks on moolide arv samaaegselt võrdne massi ja molaarmassi jagatisega. Täpselt selline näeb välja Mendelejevi-Clapeyroni võrrand. See annab selge ettekujutuse, millise süsteemi ideaalne gaas moodustab. Ideaalse gaasi olekuvõrrand on järgmine: pV=mRT/M.
Järeldage rõhu valem
Teeme saadud avaldistega veel mõned manipulatsioonid. Selleks korrutatakse Mendelejevi-Clapeyroni võrrandi parem pool ja jagatakse Avogadro arvuga. Nüüd vaatame hoolik alt aine koguse korrutist Avogadro numbri järgi. See pole midagi muud kui molekulide koguarv gaasis. Kuid samal ajal on universaalse gaasikonstandi ja Avogadro arvu suhe võrdne Boltzmanni konstandiga. Seetõttu saab rõhu valemid kirjutada järgmiselt: p=NkT/V või p=nkT. Siin on sümbol n osakeste kontsentratsioon.
Ideaalsed gaasiprotsessid
Molekulaarfüüsikas on selline asi nagu isoprotsessid. Need on termodünaamilised protsessid, mis toimuvad süsteemis ühe konstantse parameetri juures. Sel juhul peab ka aine mass jääma konstantseks. Vaatame neid täpsem alt. Niisiis, ideaalse gaasi seadused.
Rõhk jääb konstantseks
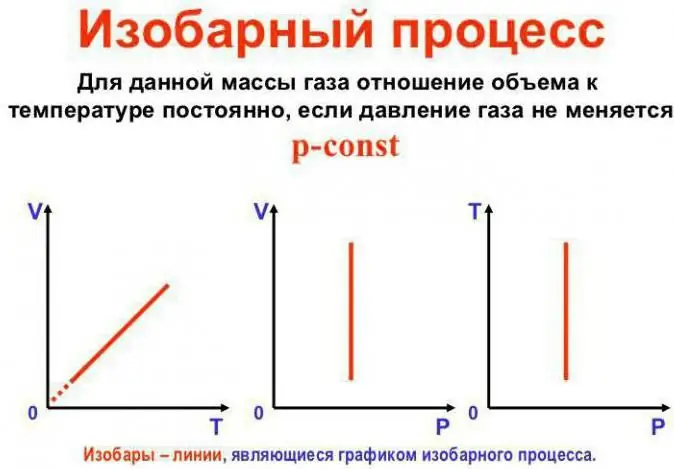
See on Gay-Lussaci seadus. See näeb välja selline: V/T=konst. Seda saab ümber kirjutada muul viisil: V=Vo (1 + at). Siin on a võrdne 1/273,15 K^-1 ja seda nimetatakse "mahu laienemise koefitsiendiks". Võime asendada temperatuuri nii Celsiuse kui kaKelvini skaala. Viimasel juhul saame valemi V=Voat.
Helitugevus jääb samaks

See on Gay-Lussaci teine seadus, mida sagedamini nimetatakse Charlesi seaduseks. See näeb välja selline: p/T=konst. On veel üks sõnastus: p=po (1 + at). Teisendusi saab läbi viia vastav alt eelmisele näitele. Nagu näete, on ideaalse gaasi seadused mõnikord üksteisega üsna sarnased.
Temperatuur püsib konstantne

Kui ideaalse gaasi temperatuur jääb konstantseks, saame Boyle'i-Mariotte'i seaduse. Selle saab kirjutada nii: pV=const.
Seotud kontseptsioon nr 2: osaline rõhk
Oletame, et meil on gaasiga anum. Sellest saab segu. Süsteem on termilises tasakaalus ja gaasid ise ei reageeri üksteisega. Siin tähistab N molekulide koguarvu. N1, N2 ja nii edasi, vastav alt molekulide arv segu igas komponendis. Võtame rõhuvalemi p=nkT=NkT/V. Seda saab avada konkreetse juhtumi jaoks. Kahekomponendilise segu korral on valem järgmine: p=(N1 + N2) kT/V. Siis aga selgub, et kogurõhk summeeritakse iga segu osarõhkudest. Seega näeb see välja nagu p1 + p2 ja nii edasi. Need on osalised rõhud.
Mille jaoks see on mõeldud?
Saadud valem näitab, et rõhk süsteemis pärineb igast molekulirühmast. Muide, see ei sõltu sellestteised. D alton kasutas seda hiljem tema järgi nimetatud seaduse sõnastamisel ära: segus, kus gaasid omavahel keemiliselt ei reageeri, on kogurõhk võrdne osarõhkude summaga.






